연구 성과 각 각 세계적 학술지 온라인판에 게재

경희대학교(총장 한균태) 장대식 약학대학 교수가 기초과학연구원(IBS)과 공동연구 결과를 공개했다. 그는 우리나라의 자생식물인 벌개미취(Aster koraiensis Nakai)와 더덕(Codonopsis Ianceolata Trautv)에서 분리한 사포닌들이 코로나바이러스 감염을 억제하는 매커니즘을 규명했다. 벌개미취에 함유된 ‘아스터사포닌 I(Astersaponin I)’과 더덕에 함유된 ‘란세마사이드 A(Lancemaside A)' 사포닌을 연구했고, 이들이 코로나바이러스의 세포 내 침입의 주요 기작인 세포막 융합을 저해해 세포 내 감염을 억제함을 새롭게 규명했다. 관련 연구 성과는 국제학술지 ’항바이러스 연구(Antiviral Research)' 10월 온라인판과 ‘항균제 및 화학요법(Antimicrobial Agents and Chemotherapy)' 11월 온라인판에 각각 게재됐다.
벌개미취와 더덕 사포닌, 코로나바이러스의 외피막과 인체세포 세포막 사이의 ’막 융합‘ 저해

벌개미취는 국화과의 여러해살이풀로 고려쑥부쟁이라고도 불린다. 제주도와 강원도 이남까지 분포하는데, 우리나라에서만 자라는 한반도 고유식물이다. 더덕은 우리에게 익숙한 산채류이다. 우리나라 전역의 산과 들에서 자라고, 도라지에 이어 우리나라에서 두 번째로 많이 재배된다. 이러한 천연물 유래 약재는 우리가 쉽게 접할 수 있고, 오랜 기간 사용돼 안정성도 입증됐다. 항생제 페니실린이나 항암제 탁솔, 말라리아 치료제 성분인 아르테미시닌 등이 천연물질에서 유래한 것으로 알려져 있다.
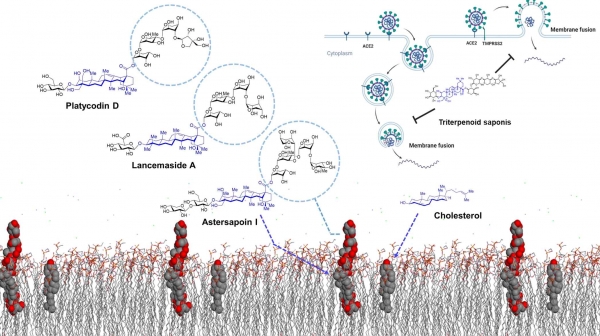
코로나바이러스의 입자는 엔도좀(endosome)이나 세포표면 형질막과 융합해 인체세포 내로 들어온다. 엔도좀은 물질 이동에 관여하는 세포 내 소포(vesicles)이다. 세포막을 통해 세포가 외부 물질을 흡수하는 ’세포 내 이입(endocytosis)’로 생성된다. 엔도좀과 세포표면 형질막 융합 경로는 공통점이 있다. 코로나바이러스의 외피막과 인체세포의 세포막 사이의 ‘막 융합’ 과정이 그것. 공동연구팀은 아스터사포닌 I와 란세마사이드 A가 이 막 융합을 저해해 코로나바이러스 세포 내 감염경로를 모두 차단함을 밝혔다.
아스터사포닌 I와 란세마사이드 A는 중앙골격구조가 세포막의 주요구성물질인 콜레스테롤과 매우 유사한데, 한쪽에 당이 길게 붙어 있다. 이 사포닌의 중앙부를 세포막 안으로 받아들이고 당 부위가 세포막 밖으로 돌출되면, 이 부분이 코로나바이러스 외피막과의 막융합을 저해한다.
막 융합 저해물질, 코로나바이러스와 세포 수용체 결합력 저해해 바이러스 감염 막아
오미크론과 같은 변이 코로나바이러스는 스파이크 단백질의 돌연변이다. 세포 수용체 ACE2와의 결합력이 높아, 세포감염력이 높은 점이 특징이다. 하지만 코로나바이러스 스파이크 단백질과 ACE2의 결합력이 높아도 결합 이후의 막 융합 과정을 막으면 코로나바이러스의 세포 내 유입을 막을 수 있다. 막 융합 저해물질이 코로나바이러스와 ACE2 결합력과 상관없이 바이러스 감염을 막는 장점이 있다.
이 연구 결과는 국제학술지 <항바이러스 연구(Antiviral Research)> 10월 온라인판과 <항균제 및 화학요법(Antimicrobial Agents and Chemotherapy)’ 11월 온라인판에 각각 게재됐다. 이번 연구에는 장대식 교수와 함께 김승택 한국 파스퇴르 연구소 박사 연구팀이 공동으로 참여했다. IBS 연구팀은 2021년 도라지 사포닌인 ‘플라티코딘 D(Platycodin D)’의 항 코로나 활성을 규명했었다. 이 연구는 같은 해 5월 국제학술지 <실험분자의학(Experomental & Molecular Medicine)>에 게재한 바 있다. 본 연구는 이 연구의 후속 연구로써 진행됐다. 아스터사포닌 I, 란세마사이드 A, 플라티코딘 D는 모두 ‘트라이터페노이드 사포닌(Triterpenoid saponin)’에 속하고, 한쪽에 당이 길게 붙어 있는 비슷한 화학구조를 가졌다는 공통점이 있다.
장대식 교수 공동연구팀의 연구는 또 다른 연구의 영감을 줬다. 한순규 KAIST 화학과 교수 연구팀은 공동으로 코로나바이러스 감염 억제 활성이 2배 향상된 유도체 합성에도 성공했다. 향후에 항바이러스 치료제에 활용할 가능성도 기대할 수 있다. 이 연구 결과는 국제학술지 <생유기화학(Bioorganic Chemistry)> 10월호에 게재됐다.
장대식 교수, “연구 결과가 국내 자생·재배 식물 활용 의약품 개발 연구 활성화에 기여하길”
장대식 교수는 “중국의 경우, 중국전통의학연구원 투유유 교수가 개똥쑥에서 말라리아 치료제인 아르테미시닌을 개발한 공로로 2015년 노벨생리·의학상을 수상한 이후 정부차원에서 중의약 연구에 전폭적인 지원을 해오고 있으나 우리나라의 경우 오히려 축소되고 있는 현실이 아쉽다”며 “이번 연구 결과 발표가 국내 자생 혹은 재배 식물을 활용한 의약품 개발 연구 분야의 활성화에 기여하길 기대한다”라고 전했다.
IBS 이창준 소장은 “벌개미취, 더덕, 도라지 및 이에 포함된 트라이터페노이드 사포닌은 일상에서 쉽게 접할 수 있는 식품 및 생약의 주요성분으로, 섭취 시상기도의 상피세포에 고농도로 노출될 수 있어 무증상환자나 초기 환자에게 효과를 기대할 수 있다”며 “아직 세포실험 단계의 연구 결과이지만 동물실험에서도 좋은 결과가 나온다면 임상실험도 가능할 것”이라고 전망했다.
IBS 김태영 선임연구원은 “지난 20년간 전 세계는 코로나바이러스로 인해 세 차례의 팬데믹을 경험했다”며 “현재 진행 중인 코로나19 팬데믹과 미래에 닥칠 수 있는 또 다른 팬데믹에 대비해 범용적 코로나바이러스 감염증 치료제 개발이 매우 절실한 상황”이라고 전했다. 이어 “막융합 저해제는 코로나바이러스와 같이 외피막 바이러스의 감염을 범용적으로 차단할 수 있으므로, 이번 연구 결과로 범용적 항바이러스 치료제 개발의 가능성을 제시했다”고 연구의 의의를 밝혔다.
 번역 제공
번역 제공

